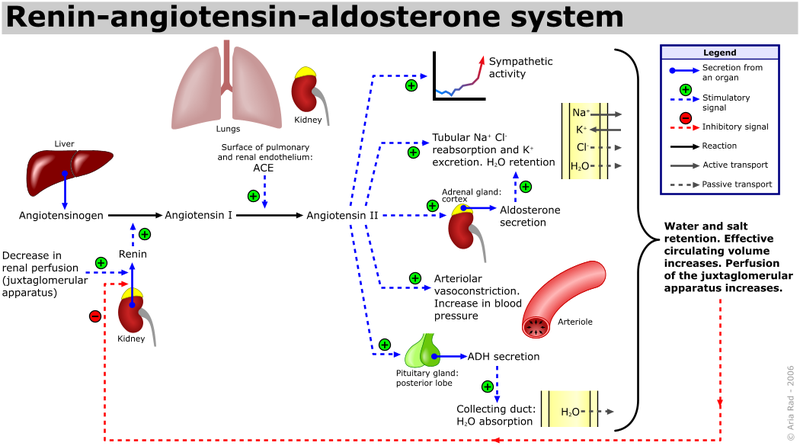
los riñones desempeñan un papel importante en el mantenimiento de la presión arterial. cuando disminuye la tensión arterial los riñones responden liberando renina que a través de la generación de angiotensina II, se traduce en un aumento del volumen plasmático y de la tensión arterial.
una caída de la tensión arterial provoca también una aumentada actividad simpática que provoca también una vasoconstricción de la arteriolas aferentes del glomérulo y una disminución en la filtración glomerular
un aumento de los niveles tensiónales ocasiona un mayor grado de filtración glomerular y una mayor perdida de líquidos a través de la orina ocasionando una reducción de la tensión arterial.
la disminución del riego sanguíneo al riñón (isquemia renal) provoca la liberación de renina por el aparato yuxtaglomerular. esta enzima desdobla un sustrato proteico en el plasma (angiotensinogeno) el cual se convierte en angiotensina I, que esta constituida por diez aminoácidos.
sobre la angiotensina I actúa la enzima convertidor de angiotensina (ECA) formando la angiotensina II que solo posee 8 aminoácidos que constituye un potente agente vasoconstrictor por actuar sobre receptores en el musculo liso de las arteriolas denominados receptores AT-1.
la angiotensina II por otra parte incrementa la secreción de ADH y aldosterona, resultando en el aumento del volumen plasmático y de una elevación de la presión arterial


- Equilibrio ácido-base
El equilibrio ácido-base se define como "aquella situación de equilibrio establecido en el balance entre sustancias de carácter ácido y básico de la sangre como consecuencia de la interacción entre los sistemas respiratorios y metabólicos"
Los valores normales son:
Sangre arterial = 7.35 / 7.45
Sangre venosa = 7.31 / 7.41
Las alteraciones encontradas en el equilibrio ácido-base pueden ser de dos tipos:
- Respiratorias: aquellas en los que la concentración de dióxido de carbono o ácido carbónico constituye el cambio primario del pH.
- Metabólicas: por una alteración en la concentración de bicarbonato
- Regulación del equilibrio ácido-base
Debido a los constantes procesos fisiológicos del organismo se generan diariamente una gran cantidad de sustancias de carácter ácidos y básicos susceptibles de alterar el equilibrio.
Dicha alteración se traduce en cambios de pH del organismo. Evitar estas variaciones es tarea de los tampones (sistemas amortiguadores) presentes en el organismo y son capaces de captar o ceder protones como respuesta a los cambios de acidez de los líquidos orgánicos.
La labor de estos tampones se desarrolla en los pulmones y riñones. En condiciones normales, el dióxido de carbono suele excretarse a través de los pulmones. Por su parte, los riñones eliminan mediante la excreción tubular los protones originados como consecuencia de las principales fuentes metabólicas (no respiratorias) y que son fundamentalmente la oxidación incompleta de grasas e hidratos de carbono y la oxidación del azufre y de los metabolitos que contienen fósforo.
Alteraciones del equilibrio ácido-base
La mayor parte de los métodos que se utilizan actualmente para determinar la existencia de un desequilibrio ácido-base en el organismo, están basados en la aplicación de la ecuación de Henderson-Hosselbach.
Para un ácido débil (HA)
[ HA ] [ H+ ] + [ A¬ ]
[ H+ ] = [ HA ]
[ A¬ ]
por lo tanto:
pH = pKa + log [ A¬ ]
[ HA ]
donde pKa = log 1
Ka
Esta expresión es considerada la ecuación "estándar" de Henderson-Hasselbach y puede ser aplicada en el caso particular para determinar las variaciones sufridas por el equilibrio ácido-base del organismo.
Concretamente, en el caso del ácido carbónico de la sangre, la reacción que tiene lugar en el plasma es:
[ H2O ] + [ CO2 ] [ H2CO3 ]
[ H2CO3 ] [ HCO3¬ ] + [ H+ ]
Aplicando la ecuación:
PH = pKa + log [ HCO3¬]
[ H2CO3 ]
Los protones que como consecuencia de un deteriorado proceso orgánico puedan ser liberados, son temporalmente tamponados por los distintos sistemas amortiguadores existentes en le organismo.
Cuando la cantidad de protones a neutralizar es excesiva pueden generarse alteraciones del equilibrio de distinta gravedad que, en ocasiones, llegan a ser incluso incompatibles con la vida. Estos desequilibrios pueden ser excesos o defectos y generan en el organismo dos estados denominados "acidosis y alcalosis"
- Acidosis: es un exceso de protones en la sangre por encima de 44 nmol/l
- Alcalosis: es un déficit de protones en la sangre por debajo de 35 nmol/l
- Valoración clínica de las alteraciones del equilibrio ácido-base
Para poner de manifiesto la existencia en el organismo de una situación de acidosis o alcalosis no es suficiente con determinar el ácido carbónico presente en el plasma ya que:
- un valor bajo de ácido carbónico plasmático puede ser debido tanto a una acidosis no primaria, como en una alcalosis primaria.
- un valor alto de ácido carbónico en el plasma puede tener su origen en una alcalosis no primaria como en una acidosis primaria.

1 comentario:
Gracias! Te felicito, es un buen aporte. tambien soy uasdiana.
Publicar un comentario